Techniques de laboratoire
Le principe de la congélation, que ce soit pour l’ovocyte ou l’embryon repose sur le passage de l’eau intra et extra cellulaire de l’état de phase liquide à l’état solide (ou vitreux) en utilisant des agents moléculaires dits cryoprotecteurs (CPs). Le rôle majeur de ces CPS sera de se substituer à l’eau intracellulaire (CPs pénétrants) en créant un gradient osmotique à l’aide d’un sucre non pénétrant (en général, le sucrose). Il existe deux procédures de congélation, la congélation lente et la vitrification. La différence principale réside en l’augmentation de la concentration en CPs lors de la vitrification qui permettra une vitesse de descente en température ultra rapide, évitant le réarrangement moléculaire de l’eau à savoir la phase cristalline. La cristallisation aléatoire de l’eau dans l’échantillon congelé est en effet principalement responsable du phénomène de lyse partielle ou totale de l’ovocyte ou embryon congelé. Observée au décours de la décongélation, cette lyse définit les paramètres qualifiant l’efficacité biologique de la procédure, à savoir principalement : le taux de survie intacte (TSI) (% d’ovocytes et/ou embryons ayant résisté totalement). Aujourd’hui, la vitrification a largement supplanté la congélation lente et permet d’atteindre un TSI >80% concernant l’ovocyte et >90% pour l’embryon, à tous les stades de son développement. Cette technique, autorisée en France depuis 2011, a révolutionné l’Assistance Médicale à la Procréation et permet aujourd’hui d’envisager sereinement la préservation de la fertilité en cas de cancers ou autres pathologies la justifiant.
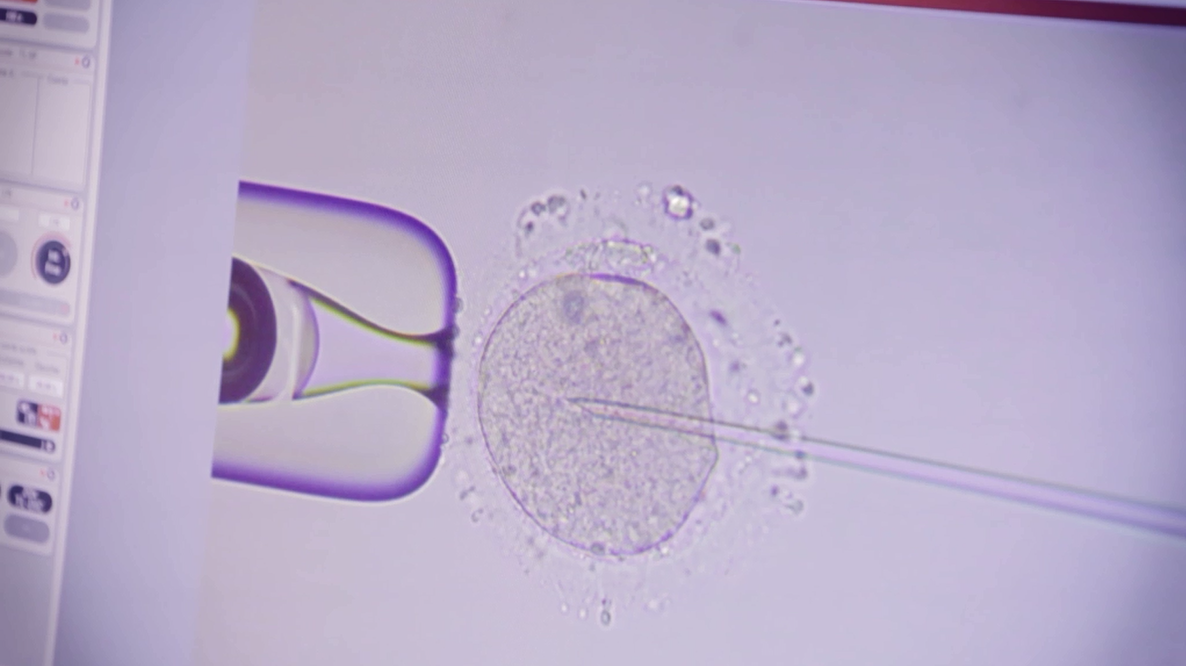
L’objectif principal de la ponction ovarienne, qu’elle suive une stimulation hormonale ou une maturation in vitro (MIV), est de recueillir le nombre adéquat d’ovocytes. Les ovocytes matures, au stade métaphase 2 de méiose, sont obtenus le jour de la ponction pour une stimulation et jusqu’à 48 heures après cette ponction concernant la MIV (après incubation dans un milieu de culture adapté). Si la femme n’est pas en couple au moment de la préservation de sa fertilité, seule la vitrification des ovocytes matures sera effectuée au laboratoire. Si cette femme est en couple, l’option de féconder tout ou partie de ses ovocytes matures avec le sperme de son conjoint lui est permise. Afin d’éviter tout risque d’échec de fécondation, le processus d’insémination des ovocytes est généralement l’ICSI (IntraCytoplasmic Sperm Injection), consistant à déposer à l’aide de micropipettes appropriées un spermatozoïde vivant dans le cytoplasme de chaque ovocyte au stade métaphase 2. Le lendemain, le rapport du nombre d’ovocytes fécondés (zygotes ou 2PN) par le nombre d’ovocytes « injectés » déterminera le taux de fécondation. Ce taux de fécondation est en moyenne >60%. Les zygotes pourront être ensuite cultivés dans des conditions strictement contrôlés au laboratoire jusqu’à différents stades dits précoces (Jours 2 et/ou 3 : embryon stade 4 et 8 cellules, respectivement) ou tardifs (Jours 5 et/ou 6 : embryon stade blastocyste). La préservation de la fertilité sera assurée par la vitrification des embryons de bonne qualité obtenus.
Il est très important de rappeler aux couples pris en charge pour préservation de la fertilité la réglementation en vigueur concernant la filiation des gamètes ou embryons, afin qu’ils se déterminent en conscience sur les conséquences possibles de leur choix. Les ovocytes vitrifiés appartiennent à la femme qui pourra donc en disposer si besoin lorsque guérie de sa maladie. Les embryons, quant à eux, appartiennent aux couples et non à la femme seule. Ainsi, leur utilisation future suppose obligatoirement que le couple soit encore constitué lors de leur éventuelle décongélation.